(一) 综述
1. 医疗器械(非体外诊断试剂,主要指无源医疗器械、有源医疗器械)
依据 《医疗器械监督管理条例(国务院 680 号令)》,第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实行产品注册管理。在无法确定医疗器械的类别时,可以采取以下几种方式:
2. 体外诊断试剂
依据 《体外诊断试剂注册管理办法》,第一类体外诊断试剂实行备案管理,第二类、第三类体外诊断试剂实行注册管理。
在无法确定体外诊断试剂的类别时,可以采取以下几种方式:
• 可以按照《体外诊断试剂注册管理办法》中的分类要求或已上市同产品进行查询
• 直接按照第三类体外诊断试剂申报
• 申请分类界定
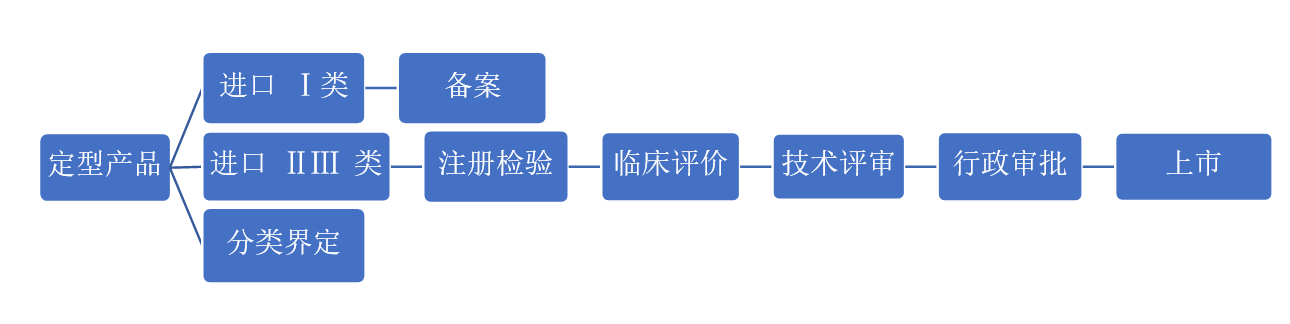
1. 医疗器械(非体外诊断试剂,主要指无源医疗器械、有源医疗器械)
依据 《医疗器械监督管理条例(国务院 680 号令)》,第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实行产品注册管理。
在无法确定医疗器械的类别时,可以采取以下几种方式:
• 可以按照《医疗器械分类规则》、《医疗器械分类目录》或已上市同产品进行查询
• 直接按照第三类医疗器械申报
• 申请分类界定
• 对于药械组合产品,需要申请属性界定
2. 体外诊断试剂
依据 《体外诊断试剂注册管理办法》,第一类体外诊断试剂实行备案管理,第二类、第三类体外诊断试剂实行注册管理。
在无法确定体外诊断试剂的类别时,可以采取以下几种方式:
• 可以按照《体外诊断试剂注册管理办法》中的分类要求或已上市同产品进行查询
• 直接按照第三类体外诊断试剂申报
• 申请分类界定